CellCentricCellCentric Ltd. · First-in-Class p300/CBP Inhibitor · Clinical-Stage Oncology
케임브리지 대학교의 후성유전학 연구실에서 탄생한 임상 단계 바이오텍 — 암 세포의 유전자 발현을 제어하는 세계 최초의 경구용 p300/CBP 저해제 인오브로딥(Inobrodib)을 개발하며, 다발성 골수종(Multiple Myeloma) 치료의 패러다임 전환을 추진하고 있다. 2026년 5월 오버서브스크라이브드 $2.2억 Series D를 완료, 피보탈 임상 진입과 독립적 상업화 경로를 확보했다.
CellCentric은 2003년 케임브리지 대학교의 발생생물학자 Prof. Azim Surani FRS, CBE가 스핀아웃(Spin-out) 형태로 창립하고, Will West Ph.D.가 공동 창업자 겸 CEO로 경영을 주도하며 발전시킨 임상 단계 바이오테크 기업입니다. 창립의 출발점은 Surani 교수가 규명한 후성유전학(Epigenetics)의 발견 — DNA 서열 외의 유전 코드가 세포의 운명(Cell Fate)을 결정한다는 원리 — 으로, 이를 치료학적으로 활용할 수 있다면 암의 핵심 유전자 발현 자체를 표적으로 삼는 전혀 새로운 범주의 항암제가 가능하다는 통찰에 있습니다. CellCentric은 이 기초과학적 발견을 출발점으로 20여 년간 50개 이상의 후성유전학 표적을 탐색하고, 최종적으로 p300/CBP 저해라는 단일 핵심 프로그램에 집중하여 세계 최초의 경구용 p300/CBP 저해제 인오브로딥(Inobrodib)을 개발했습니다.
케임브리지 대학교 거든 연구소(Gurdon Institute)의 발생생물학 교수인 Surani 교수는 후성유전학(Epigenetics) 현상을 세계 최초로 보고한 과학자 중 한 명입니다. 그는 DNA 서열 이외에도 유전되는 코드 — 즉 세포의 운명을 지시하는 후성유전학적 조절 메커니즘 — 가 존재함을 발견하고 기술했습니다. 이로부터 히스톤(Histone)과 전사 공동활성화 인자(Transcription Co-activation Factor)를 조절하는 효소들이 새로운 약물 발견의 미개척 표적이 될 수 있다는 가설이 출발했으며, CellCentric은 이 과학적 토대를 상업화하기 위해 설립되었습니다.
Surani 교수는 영국 왕립학회 석학회원(FRS)이자 대영제국 훈장(CBE) 수훈자로, 학문적 독창성과 사회적 기여를 동시에 인정받은 세계적 생명과학자입니다. CellCentric의 창립 이후에도 과학자문위원회(Scientific Advisory Board) 등을 통해 회사의 기초과학 방향성에 지속적으로 기여하고 있습니다.
Will West는 CellCentric의 공동 창업자이자 현 최고경영자(CEO)로, 회사의 설립 초기부터 임상 단계까지 전략적 성장을 이끌어온 핵심 인물입니다. 그는 후성유전학 기반 약물 발견에서 임상 개발, 투자 유치, 미국 시장 진출에 이르는 CellCentric의 전 과정을 총괄 지휘했습니다. 2024~2025년에 걸쳐 Pfizer, RA Capital, Forbion 등으로부터 누적 $400M 이상을 조달하며 영국의 소규모 연구 중심 스타트업을 글로벌 피보탈 임상 역량을 갖춘 트랜스대서양 바이오테크로 전환시켰습니다.
CEO로서 그는 “환자가 지역 사회에서 직접 복용할 수 있는 경구 항암제”라는 제품 철학을 일관되게 관철하여, 복잡한 입원 치료 없이 다발성 골수종 환자가 자택에서 복용 가능한 혁신적인 치료 옵션을 지향해 왔습니다. 2025년 Burlington, MA(보스턴 인근)에 미국 오피스를 개설하며 FDA 규제 전략 및 상업화 준비를 본격화했습니다.
CellCentric의 창립 과정은 전형적인 “아카데믹 스핀아웃”의 경로를 따릅니다. Surani 교수의 후성유전학 발견이 “어떤 단백질을 어떻게 억제하면 암 세포의 유전자 발현을 제어할 수 있는가?”라는 약물 발견의 질문으로 전환되고, 회사는 약 15~20년의 기간 동안 50개 이상의 후성유전학 표적을 탐색한 끝에 p300/CBP 브로모도메인 저해라는 단일 핵심 메커니즘으로 수렴했습니다. 이 집중화(Focus)의 결과가 바로 인오브로딥입니다. Takeda에 기술 이전한 아르기닌 메틸전이효소(Arginine Methyltransferase) 프로그램 등 다수의 파이프라인을 파트너링하며 사업 지속성을 확보한 것도 이 단계의 핵심 전략이었습니다.
“Inobrodib is a new modality and a potential fresh option for patients that is orally administered. We must serve the widest possible communities of patients, and as an oral, well-tolerated drug that can be taken at home, inobrodib has an important role to play.”
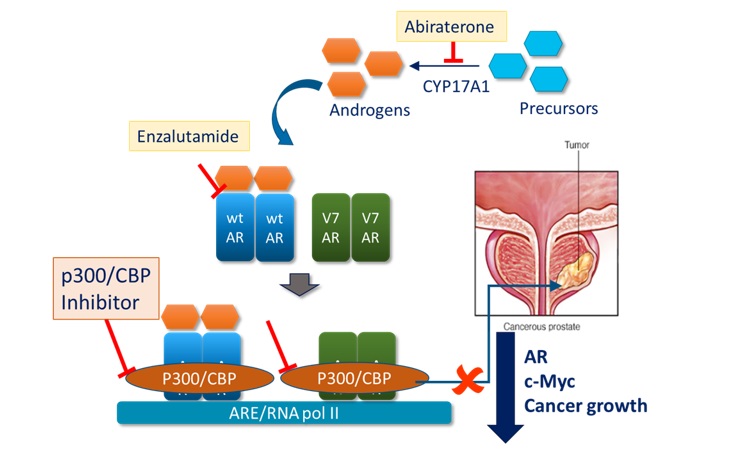
CellCentric의 핵심 자산은 세계 최초의 경구용 p300/CBP 브로모도메인 저해제(Bromodomain Inhibitor)인 인오브로딥(Inobrodib, 구 CCS1477)입니다. 인오브로딥은 p300과 CBP라는 두 개의 평행 단백질(Paralogue)이 초강화인자(Super Enhancer) 부위에 결합하는 것을 차단하여 암의 핵심 구동 유전자인 MYC와 IRF4의 발현을 억제합니다. 기존의 표적 저해 또는 단백질 분해(Degradation) 방식과 달리 표적 대체(Target Displacement) 메커니즘으로 작용하는 것이 학문적으로 검증된 독창적 작용 원리입니다(Cancer Cell, 2023).
평가 환자 수
InoPd 반응률 향상 (ASH 2025)
사이트 지역
혈액암(다발성 골수종, 비호지킨 림프종, 급성 골수성 백혈병, 고위험 골수이형성증후군)과 다양한 고형암 환자 500명 이상을 대상으로 단독 요법의 안전성·내약성·용량 설정을 완료했습니다. 권고 2상 용량(RP2D)에서 일관된 임상 활성이 확인되었으며, 대부분의 독성 반응은 경미하거나 중등도 수준으로 관리 가능한 것으로 평가됩니다. 경구 캡슐 형태로 자택 복용이 가능하며 집중적인 모니터링이 불필요한 것이 핵심 임상적 차별성입니다.
CellCentric의 핵심 상업화 경로입니다. 2025년 12월 ASH에서 발표된 Phase 2 용량 최적화 데이터에서, 인오브로딥 20mg과 표준 용량 포말리도마이드·덱사메타손의 병용 요법(InoPd)은 중위 5차 이전 치료력을 보유한 중증 재발·불응성 다발성 골수종(RRMM) 환자에서 기존 대체 요법 대비 2배 이상의 반응률을 달성했습니다. 2026년 3월 영국·미국에서 DOMMINO-1 첫 환자 투여를 개시했으며, 2026년 하반기 글로벌 Phase 3 DOMMINO-2 개시를 통해 등록 가능 연구(Registration-enabling Study) 완료를 목표로 합니다. 완전 경구 3중 요법(All-oral Triplet)이라는 점이 기존 주사 기반 치료와의 핵심 차별점입니다.
BCMA×CD3 이중특이 T세포 관여항체(Bispecific T Cell Engager)인 Pfizer의 Elrexfio(elranatamab) 및 J&J의 Tecvayli(teclistamab)와의 병용 가능성을 탐색 중입니다. 기존 이중특이항체 치료 후 내성 또는 불내성 환자군 — CellCentric이 “중요하고 성장하는 미충족 수요”로 정의하는 집단 — 에서의 구제 요법(Salvage) 또는 추가 차선 치료(Later-line) 가능성을 평가합니다. CellCentric은 인오브로딥에 대한 모든 개발 및 상업 권리를 독점 보유하고 있어 병용 파트너 확장에 제약이 없습니다.
암의 재발을 억제하는 유지 요법으로서 인오브로딥의 가능성을 탐색하고 있습니다. 경구 복용이 가능하고 내약성이 우수한 인오브로딥의 특성은 장기 유지 요법에 이상적인 프로필이며, 이 적응증이 성공할 경우 다발성 골수종 치료의 전 단계(Earlier Line)에 인오브로딥을 포지셔닝할 수 있는 핵심 전략입니다. 임상적 성공 시 단순한 후기 구제 요법을 넘어 전반적인 다발성 골수종 치료 패러다임에서의 역할이 크게 확대됩니다.
최초 임상 데이터 공개. RRMM 26명 단독요법에서 RP2D 7명 중 6명 반응 확인. 다발성 골수종 임상 활성 첫 공개 검증.
재발·불응성 다발성 골수종 치료에 대한 FDA 패스트 트랙(Fast Track) 및 희귀의약품(Orphan Drug) 이중 지정 획득. 가속 심사 경로 확보.
Phase IIa에서 InoPd 75% 전체 반응률(ORR) 발표. 포말리도마이드와의 상가적(Additive) 효과 메커니즘 검증(Blood Cancer Discovery).
Phase 2 용량 최적화 데이터: InoPd 20mg이 기존 대체 요법 대비 2배+ 반응률. 중등 독성 프로필 확인. Series D 투자 유치의 핵심 근거 데이터.
영국·미국에서 DOMMINO-1 첫 환자 투여 완료. 피보탈 Phase 2 임상 공식 개시. 등록 연구(Registration Study) 단계 진입.
글로벌 Phase 3 DOMMINO-2 개시 예정. FDA 승인 신청(NDA/BLA)을 위한 최종 등록 연구. Series D 자금의 핵심 사용처.
다발성 골수종은 혈액암 중 두 번째로 흔한 암으로, 글로벌 시장은 2034년까지 약 $500억 규모로 성장이 전망됩니다(GlobeNewswire, 2025). 최근 다수의 이중특이항체 및 CAR-T 치료제가 승인되며 치료 옵션이 확장되었으나, 대부분의 환자는 결국 재발(Relapse)하며 기존 치료에 불응성(Refractory)이 됩니다. 특히 BCMA/TCE 기반 이중특이항체 치료 이후 재발한 환자군은 현재 표준적인 치료 대안이 부재하며, 이 집단이 바로 CellCentric이 DOMMINO 임상을 통해 직접 공략하는 미충족 의료 수요의 핵심입니다. 또한 인오브로딥은 복잡한 병원 인프라 없이 자택에서 복용할 수 있어 지역사회(Community Setting) 환자 접근성을 획기적으로 개선합니다.
CellCentric의 투자 유치 여정은 아카데믹 기초과학 연구에서 출발해 전략적 제약사 파트너십을 거쳐 전문 헬스케어 기관투자자 중심의 피보탈 임상 파이낸싱으로 발전하는 전형적인 바이오테크 성숙 궤적을 보여줍니다. 특히 2023~2026년의 3년간 Pfizer의 전략 투자($25M), RA Capital 리드 시리즈($35M + $120M), 그리고 최종 오버서브스크라이브드 $220M Series D까지 총 $400M 이상을 조달하며, 임상 데이터의 품질이 자본 유치를 주도하는 선순환 구조를 확립했습니다.
(2023)
(2024)
(2025.05)
(2026.05)
CellCentric은 창립 이후 20여 년 동안 Morningside Venture Capital(홍콩 기반 글로벌 생명과학 투자사) 등을 통해 연구 개발 자금을 확보하는 한편, Takeda Pharmaceuticals에 아르기닌 메틸전이효소(Arginine Methyltransferase) 약물 발견 프로그램을 기술 이전·라이선싱함으로써 사업 지속성을 유지했습니다. 또한 BrightEdge(미국암학회 임팩트 투자·벤처캐피털 부문)가 초기부터 투자에 참여하며 CellCentric의 사회적 사명 — 환자 접근성 개선과 치료 형평성 향상 — 에 대한 기관의 신뢰를 표명했습니다. 이 기간은 p300/CBP 저해 메커니즘의 과학적 검증과 인오브로딥의 임상 진입 준비 기간에 해당합니다.
2023년 7월, 세계 최대 제약기업 중 하나인 Pfizer가 $2,500만 달러의 전략적 투자(론 노트 형태, 후에 지분으로 전환)를 단행했습니다. 이 투자는 단순한 재무적 참여를 넘어, Pfizer가 자사의 다발성 골수종 치료제 Elrexfio(elranatamab)와 인오브로딥의 병용 가능성을 공동 탐색하는 전략적 제휴의 성격을 포함했습니다. Pfizer의 참여는 세계 수준의 제약 전문가들이 인오브로딥의 임상적 가치와 상업화 잠재력을 인정했다는 외부 검증(External Validation)으로, 이후 기관투자자 유치의 강력한 근거가 됩니다. 또한 Irena Melnikova (Pfizer Ventures Partner)가 이사회에 합류하며 전략적 연계를 제도화했습니다.
RA Capital Management(보스턴 기반 다단계 생명과학 전문 투자사)가 $3,500만 달러를 투자하며 CellCentric의 주요 재무 파트너로 등장했습니다. 동시에 Pfizer의 기존 $2,500만 론 노트가 지분으로 전환되어 총 $6,000만 이상의 자본이 확충됐습니다. 또한 미국암학회 BrightEdge가 $70만의 추가 투자를 집행했습니다. 이 라운드의 전략적 의미는 재무적 규모를 넘어 미국 시장 진출의 출발점이라는 데 있습니다. RA Capital은 영국에 소재한 CellCentric이 보스턴 중심의 미국 바이오텍 생태계에 편입되는 가교 역할을 했으며, Laura Stoppel (RA Capital Principal)이 이사회에 합류했습니다. 이 자금은 Phase II/III 준비 및 미국 임상 시험 확장에 활용됐습니다.
2025년 5월, CellCentric은 RA Capital Management(공동 리드)와 유럽 선도 바이오텍 VC Forbion(신규 공동 리드)이 이끄는 $1억 2,000만 Series C를 완료했습니다. Avego Bioscience Capital과 BrightEdge(미국암학회 VC)도 참여했습니다. CEO Will West는 이 조달을 “어려운 시장 환경에서 이뤄진 중요한 성과”로 평가하며, 손에 쥔 데이터의 질, 인오브로딥의 명확한 임상적·상업적 기회, 팀의 역량이 투자자 신뢰의 근거라고 밝혔습니다. 이 자금은 ① 중증 재발·불응성 다발성 골수종 환자 대상 Phase II/III 연구(가속 승인 지원 목적) 개시, ② 2026년 중반 개시를 목표한 Phase 3 프로그램 준비, ③ 이중특이항체와의 병용 탐색 임상에 배정됐습니다. Forbion의 Jasper Bos가 이사회에 합류했습니다. Burlington MA 오피스 개소와 동시에 진행된 이 라운드는 CellCentric의 트랜스대서양 전략의 완성을 의미합니다.
2026년 5월 6일, CellCentric은 수요 초과 달성(Oversubscribed) $2억 2,000만 Series D를 완료했습니다. 전문 헬스케어 투자사 Venrock Healthcare Capital Partners가 리드하고, 신규 투자자 Fidelity Management & Research Company, Sofinnova Partners, HBM Healthcare가 합류했습니다. 기존 투자자 RA Capital Management, Forbion, Pfizer, Avego BioScience Capital, BrightEdge(미국암학회)가 전원 재참여하며 연속성과 신뢰를 강화했습니다.
이번 라운드의 3대 전략적 의미:
① 피보탈 임상 완료 자금 확보 — 이미 개시된 Phase 2 DOMMINO-1(영국·미국)의 지속 모집 및 2026년 하반기 글로벌 Phase 3 DOMMINO-2 개시. FDA 등록을 위한 최종 근거 데이터 확보 목표
② 독립적 상업화 경로 수립 — CEO Will West가 “파마 딜에 집착하던 과거와 달리 이제 충분한 런웨이로 독립적 시장 진출을 추진할 수 있다”고 밝히며 인오브로딥 전 상업 권리를 독자적으로 행사할 전략 표명
③ IPO 가능성 공개 검토 — Fierce Biotech 보도에 따르면 CellCentric은 임상 성과에 따른 IPO 경로를 검토 중으로, Series D는 상장 전 최종 사전 투자(Pre-IPO) 성격을 포함
CellCentric의 방어적 경쟁력은 세계 최초의 경구용 p300/CBP 저해제로서의 선점 지위, 20년 이상 축적된 케임브리지 기반 후성유전학 지식재산(IP) 포트폴리오, 다중 임상 데이터로 검증된 인오브로딥의 상가적(Additive) 병용 효능, 경구 투여라는 환자 친화적 투여 방식, 그리고 Pfizer를 포함한 전략적 파트너 생태계에서 형성됩니다. 다발성 골수종 치료의 패러다임이 이중특이항체와 세포 치료제로 이동함에 따라 이후 내성 환자군이 구조적으로 증가하고 있으며, 인오브로딥은 바로 이 공백을 표적으로 하는 유일한 임상 단계 경구 옵션입니다.
인오브로딥은 p300/CBP 브로모도메인을 표적으로 하는 세계 최초이자 임상에 진입한 유일한 경구 저해제입니다. 케임브리지 대학교 Surani 교수 연구실에서 출발하여 20년 이상 구축된 특허 포트폴리오와, Cancer Cell·Blood Cancer Discovery 등 최고 수준 학술지에 게재된 메커니즘 논문들이 강력한 지식재산 해자를 형성합니다. 기존 BET 저해제와 명확히 구분되는 표적 대체(Target Displacement) 메커니즘 — 단백질을 분해하거나 차단하는 것이 아니라 슈퍼 인핸서 부위에서 밀어내는 방식 — 은 경쟁사가 단기간 복제하기 어려운 독자적 과학적 기반을 구성합니다.
다발성 골수종의 최신 치료 옵션인 이중특이항체 및 CAR-T 치료제는 입원 치료, 집중 모니터링, 전문 의료 시설을 필요로 합니다. 인오브로딥은 경구 캡슐로 자택에서 복용하며 집중 모니터링이 불필요합니다. 이는 단순한 편의성을 넘어 지역사회(Community Setting) 환자 접근성을 획기적으로 확대하고, 의료 시스템 전체의 비용 구조를 개선합니다. 인오브로딥의 우수한 내약성 프로필은 고령·허약 환자나 기존 치료를 감당하기 어려운 환자들에게 사실상 유일한 치료 옵션이 될 수 있음을 의미하며, 이는 규제 기관(FDA) 심사에서도 임상적 의미(Clinical Meaningfulness)로 인정받는 차별점입니다.
p300/CBP는 다발성 골수종의 핵심 구동 유전자인 MYC와 IRF4를 동시에 조절하는 유일한 단백질 쌍입니다. 기존 프로테아좀 저해제(PI), 면역조절제(IMiD), BCMA 표적 항체가 내성을 유발하는 기전과 별개의 경로를 통해 작용하므로, 다중 치료 이후 내성이 생긴 환자에서도 임상 활성이 유지됩니다. 또한 인오브로딥은 포말리도마이드(IMiD)에 내성을 보이는 암 세포를 재감작(Resensitize)시켜 IMiD 치료에 다시 반응하게 만드는 상가적 효능이 검증됐습니다(Blood Cancer Discovery, 2023). 이 특성은 내성 극복(Overcoming Resistance)이라는 미충족 수요에 직접 응답합니다.
CellCentric은 인오브로딥에 대한 모든 개발 및 상업 권리를 독점 보유하고 있습니다. 이는 병용 파트너, 시장, 적응증 확장에 제약 없이 전략을 구사할 수 있는 최대한의 유연성을 의미합니다. 동시에 Pfizer는 전략 투자자 및 병용 임상 파트너로 이미 에코시스템에 편입되어 있어, 향후 파마 딜(라이선싱, 공동 상업화, M&A 등) 또는 독자 IPO 중 유리한 경로를 선택할 수 있는 협상력을 보유합니다. CEO Will West가 Series D 이후 “독립적 시장 진출” 전략을 명시한 것은 현재 자산가치에 최대한의 프리미엄을 요구할 수 있는 자신감의 표현입니다.
$2억 2,000만 Series D를 기반으로 CellCentric의 다음 18~24개월이 시작됩니다. DOMMINO-1(Phase 2)의 데이터 성숙, DOMMINO-2(Phase 3)의 전 세계 환자 모집 개시, 이중특이항체 병용 데이터 확보, 그리고 FDA 가속 승인(Accelerated Approval) 신청 준비가 핵심 마일스톤입니다. Surani 교수가 케임브리지 연구실에서 처음 발견한 후성유전학의 원리 — DNA 외의 코드가 세포의 운명을 결정한다 — 는 이제 Venrock·Fidelity·Pfizer·RA Capital이 공동으로 신뢰하는 임상적 현실이 됐습니다. “환자가 지역사회에서 복용할 수 있는 경구 항암제로 다발성 골수종의 치료 지형을 변화시킨다”는 CellCentric의 창립 미션은, 세계 최초의 p300/CBP 저해제를 통한 실제 임상 검증이라는 이정표와 함께 현실에 성큼 다가섰습니다.